Artículos
Aplicación subcutánea en incubadora de la cepa VG/GA del virus de la enfermedad de Newcastle
13 August 2015

Merial forma parte ahora de Boehringer Ingelheim
El objetivo del presente ensayo es evaluar el patrón de replicación de la cepa VG/GA aplicada por vía subcutánea (distinta la ruta natural de infección) con la finalidad de explicar los mecanismos de la estimulación antigénica que genera los beneficios en la respuesta inmune observados por su aplicación.
.jpg)
Conferencia de Francisco Perozo, Universidad de Zulia, Venezuela; Rafael Fernández, Francisco Rojo y Héctor Garcia, Merial Select, Inc, EUA y Stephane Lemiere, Merial S.A.S., Francia. Conferencia presentada durante la XL Convención Anual ANECA, Riviera Maya, México en mayo de 2015.
El virus de la enfermedad de Newcastle (ENC) es el responsable de una de las enfermedades aviares de mayor importancia a nivel mundial (1). En países como Venezuela, Colombia y México donde la presencia de cepas virulentas en la industria avícola es endémica, se generan cuantiosas pérdidas económicas y se establecen barreras comerciales. El control de la enfermedad requiere de un diagnóstico adecuado, vacunaciones preventivas y fuertes medidas de bioseguridad (5).
En Latinoamérica y como consecuencia del alto nivel de desafío presente durante los últimos años, la vacunación por spray al día de edad con cepas que se replican tanto en el epitelio respiratorio como en el digestivo (VG/GA) (4) o de cepas enterotrópicas asintomáticas (5), acompañadas de vacunas inactivadas y revacunaciones a campo con cepas respirotrópicas mas invasivas entre los 8 y 18 días de edad, es una práctica común con buenos resultados (2).
Investigaciones recientes han demostrado que la utilización de la vía subcutánea (SC) para la aplicación de vacuna viva contra la ENC es una nueva herramienta con la que cuenta el técnico de campo para el control de la enfermedad, observándose beneficios en cuanto a la respuesta serológica y los niveles de protección contra desafíos experimentales (6).
El concepto planteado por esta línea e investigación es la aplicación subcutánea de virus vivo como la cepa VG/GA en incubadora acompañando de una vacuna vectorizada HVT-IBD, constituyéndose de esta manera en una dosis multivalente (protección contra Newcastle y Marek y Gumboro) que aprovecha las ventajas de la aplicación individual en el contexto de uniformidad y control e la vacunación que ofrece la planta de incubación (6).
El objetivo del presente ensayo es evaluar el patrón de replicación de la cepa VG/GA aplicada por vía subcutánea (distinta la ruta natural de infección) con la finalidad de explicar los mecanismos de la estimulación antigénica que genera los beneficios en la respuesta inmune observados por su aplicación. Para ello se comparó la patogenia de la cepa VG/GA aplicada por vía SC con la replicación por vía spray. Adicionalmente, se evaluó el efecto en el patrón de replicación da VG/GA de la aplicación concomitante (SC) de una vacuna vectorizada HVT-IBD diseñada para proteger contra la enfermedad de Marek y Gumboro.

Investigación sobre la vacunación subcutánea de Newcastle
Diseño del experimento
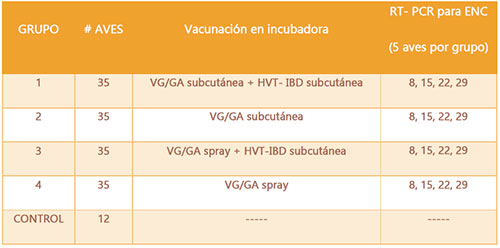
Para el ensayo se utilizaron un total de 150 aves libres de patógenos específicos (SPF) de un día de edad distribuidas en cuatro grupos experimentales y un control que se describen a continuación y se resumen en la Tabla 1.
Grupo 1 = VG/GA subcutánea + HVT-IBD subcutánea.
Grupo 2 = VG/GA subcutánea.
Grupo 3 = VG/GA spray + HVT-IBD subcutánea.
Grupo 4 = VG/GA spray.
Grupo 5 = Control no vacunado.
A los 8, 15, 22 y 29 días post vacunación se sacrificaron 5 aves por grupo y se colectaron tráqueas, bazos, e intestino delgado para detectar el virus de ENC de manera individual mediante PCR de tiempo real siguiendo protocolos estándar previamente descritos (8).
Vacunas utilizadas
Avinew® (Laboratorio Merial) vacuna a virus vivo de replicación entérica cepa Villegas/Glisson de la Universidad de Georgia (VG/GA).
VAXXITEK HVT-IBD® vacuna vectorizada de Herpesvirus de pavo con un inserto de proteína viral 2 del virus de la enfermedad de Gumboro.
Todas las vacunas se aplicaron a la dosis recomendada por el fabricante.
Tabla 1. Planes de vacunación evaluados para determinar la patogenia de la cepa VG/GA del virus de la ENC aplicado por vía subcutánea
Resultados de la vacunación
Los resultados de los niveles de detección de la cepa VG/GA del virus de la ENC se observan en las Figuras 1 a la 3. Fue posible detectar la presencia de la cepa VG/GA en diferentes órganos a distintos momentos post vacunación a pesar de haber sido colocada por vía subcutánea al día de edad que no corresponde con la ruta natural de infección del virus, lo que sugiere que el virus es transportado del punto de inoculación hasta los diferentes tejidos propiciando una estimulación antigénica en los órganos en la que es requerida para generar protección.
A los 8 días el grupo SC obtuvo niveles de detección cercanos a 80% en todos los órganos. El patrón inicial de replicación de la cepa VG/GA no difiere significativamente si se aplica por vía spray (vía respiratoria) o por vía subcutánea.
A medida que las evaluaciones se distanciaron del momento de vacunación los niveles de detección disminuyeron para ambas rutas, la disminución siendo más marcada en las aves vacunadas por vía subcutánea. El segundo objetivo era determinar si la aplicación concomitante de la VG/GA por vía subcutánea con una vacuna vectorizada podía afectar el patrón de replicación del virus de Newcastle. Según se observa en bazo e intestino no hay diferencia significativa en la detección entre los grupos vacunados con o sin la vectorizada.
Para el caso de la tráquea la comparación de los niveles de detección entre los grupos 1 y 2 (VG/GA Sc con y sin vectorizada, respectivamente) no muestra diferencias a los 8 días post vacunación pero difieren a los 15, 22 y 29 días con niveles de detección más altos en el grupo que no uso la vectorizada, este efecto no se observó en los grupos 3 y 4 donde la vacuna vectorizada se aplicó por vía subcutánea y la vacuna viva de Newcastle se aplicó en spray.
Los niveles de detección en la tráquea (Figura 1) muestran que la cepa VG/GA aplicada por vía subcutánea se replica y es detectable en el 80% de las muestras (4 / 5) a los 8 días post vacunación.
Figura 1. Niveles de detección de la cepa VG/GA en tráquea
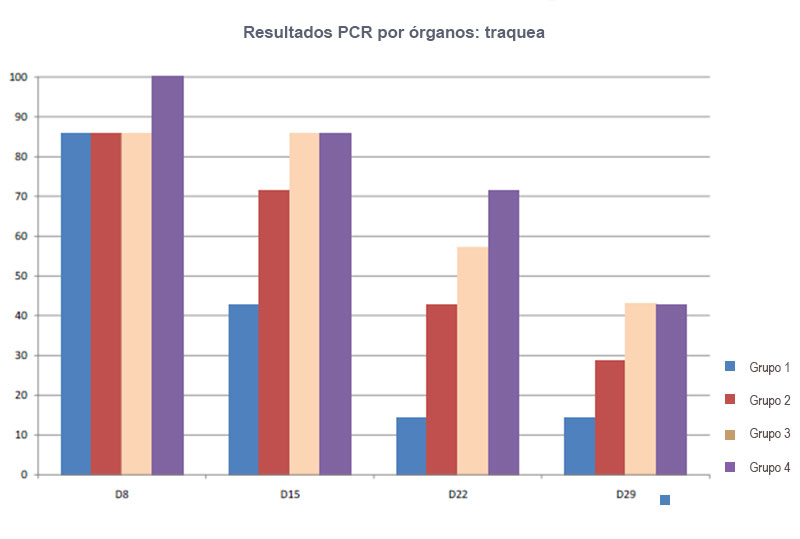
Figura 2. Niveles de detección de la cepa VG/GA en bazo
Figura 3. Niveles de detección de la cepa VG/GA en intestino
Los niveles de detección en intestino y bazo (Figuras 2 y 3) confirman que la cepa VG/GA se replica en intestino y que el virus vacunal aplicado por vía subcutánea se traslada hasta los órganos linfoides secundarios para en los centros germinales estimular una respuesta inmune. Los más altos niveles de detección corresponden a los 8 y 15 días post vacunación.
¿Cuál es la mejor vía de vacunación contra Newcastle?
Para la vacunación contra el virus de ENC, la vacuna de elección es aquella que induce una respuesta inmune protectora con un mínimo de reacciones respiratorias (1). La cepa VG/GA se replica tanto en el tracto respiratorio como en el digestivo y su nivel de protección es equivalente el proporcionado por otras cepas vacunales disponibles comercialmente, incluyendo la cepa La Sota (4).
La replicación dual de la cepa se hace excepcionalmente útil pues se replica en el tracto respiratorio sin producir reacciones post vacunales estimulando la respuesta inmune celular y la producción de Inmunoglobulinas locales (IgA) en el intestino, que es una de las principales puertas de entrada del virus velogénico viscerotropico al cual se enfrenta la industria (7).
Resultados previos de nuestro laboratorio sugieren que incluir la ruta subcutánea para la aplicación de vacunas vivas de Newcastle es útil para un programa de control efectivo de la enfermedad (6). Sin embargo, la patogenia y el mecanismo inmunológico asociado a un virus resprotrópico /enterotrópico aplicado por vía subcutánea no está completamente entendida y requiere de más información para explicarlo adecuadamente.
En el presente ensayo se demuestra que el virus aplicado SC en el cuello se distribuye rápidamente por los distintos órganos importantes para la estimulación del sistema inmunológico y la protección contra un potencial desafío de la enfermedad.
Estos resultados son consistentes con los de Peleg y col en 1993 (3), quienes demostraron que la aplicación subcutánea de virus vivo de ENC en combinación con vacuna inactivada (viva en aceite) era eficaz para el control de la enfermedad. Según el antes mencionado autor la ventaja de la vacunación subcutánea “viva en aceite” se basa en que el virus vivo se escapa de la captura de aceite que hay en su entorno y de este modo da inicio a la infección y replicación del virus en los órganos y tejidos blanco.
Esta activación del sistema inmune por un virus vivo en una etapa muy temprana de la inmunización es un evento eficaz. En resumen, los resultados de replicación y patogenia para la cepa vacunal VG/GA de ENC sugieren que indiferentemente de la ruta, el virus vivo es capaz de alcanzar sus órganos diana y estimular una respuesta inmune apropiada.
Conclusiones
Los resultados observados en este ensayo donde 8 días post vacunación las aves vacunadas por vía subcutánea (SC) muestran niveles de detección cercanos al 80% en todos los órganos, sugieren que el virus aplicado por vida SC es trasladado a los sitios idóneos para la estimulación antigénica y que los mecanismos inmunes no difieren por el cambio de ruta las conclusiones se resumen a continuación:
• El tropismo de la cepa VG/GA aparenta ser el mismo en aves vacunadas por vía subcutánea o por spray al día de edad
• A los 8 días la tasa más alta de replicación se observó en tráqueas para ambos grupos.
• No se observó interacción negativa al colocar la cepa VG/GA y la vectorizada HVT-IBD.
• En base a estos resultados se asume que la estimulación antigénica y respuesta inmune no difieren por el cambio de ruta de aplicación.
Referencias
1. Alexander, D. Newcastle Disease. Brit. Poul. Sci. 42 (1). 5-22. 2001.
2. Fernandez, R; Sol, J; Ramírez, A.. La enfermedad de Newcastle, Control y Experiencias de campo. Memorias del I Seminario de Patología Aviar. Maracaibo 20 y 21 de Octubre. Venezuela. 25 -28. 2002
3. Peleg, B; Samina, I; Brenner, J.. Inmunization of chickens with Newcastle live disease vaccine adjuvanted with oil. Vaccine. Vol XI (10): 1074-1076. 1993.
4. Perozo F, Villegas P, Dolz , R, Afonso CL, Purvis L.. The VG/GA strain of Newcastle disease virus: mucosal immunity, protection against lethal challenge and molecular analysis. Avian Pathol. 37:237–245. 2008.
5. Perozo, F. Actualidades sobre la Enfermedad de Newcastle. XXXVII Convención Nacional Aneca. Jalisco- México. 2012.
6. Perozo, F. XVII World Poultry Veterinary Association Congress. Nantes, Francia. 19-23 de Agosto 2013.
7. Perozo. F; Marcano. R Afonso, C. Biological and Phylogenetic Characterization of a Genotype VII Newcastle Disease Virus from Venezuela: Efficacy of Field Vaccination. J. Clin. Microbiology 50 (4) 1204-1208. 2012.
8. Wise, M ., et al. Development of a Real-Time Reverse-Transcription PCR for Detection of Newcastle Disease Virus RNA in Clinical Samples. J. Clin. Microbiol. 42 (1). 329-338. 2004.
También le interesaría
Efecto de las condiciones de campo en la respuesta a la vacunación contra la enfermedad de Newcastle
Agosto 2015
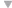

 © 2000 - 2021. Global Ag MediaNinguna parte de este sitio puede ser reproducida sin previa autorización.
© 2000 - 2021. Global Ag MediaNinguna parte de este sitio puede ser reproducida sin previa autorización.